《化學(xué)》電子教案
 
課題 | 第五章 烴和烴的衍生物 第三節(jié) 烴的衍生物(二) |
教學(xué)目標(biāo) | 1.了解乙醛的組成和結(jié)構(gòu),,理解乙醛的還原反應(yīng)、氧化反應(yīng)及乙醛的用途 2.了解乙酸的組成和結(jié)構(gòu),,理解乙酸的酸性,、酯化反應(yīng)及乙酸的用途 |
教學(xué)重點(diǎn) | 1.乙醛化學(xué)性質(zhì)及有關(guān)化學(xué)方程式的正確表示 2.乙酸的化學(xué)性質(zhì) |
教學(xué)難點(diǎn) | 乙醛、乙酸的分子結(jié)構(gòu) |
課時(shí)安排 | 2學(xué)時(shí) |
教學(xué)方法 | 對(duì)比-聯(lián)想結(jié)合方法,;啟發(fā)式教學(xué)與講練結(jié)合方法 |
教學(xué)手段 | 多媒體輔助,,課堂實(shí)驗(yàn) |
教學(xué)用具 | 投影儀,化學(xué)實(shí)驗(yàn)儀器 |
 
【教學(xué)進(jìn)程】
導(dǎo)入
前面已經(jīng)學(xué)習(xí)了乙醇,、苯酚的相關(guān)知識(shí),,今天來認(rèn)識(shí)另外一種重要的烴的衍生物——乙醛。
板書
三,、乙醛
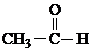
(一)乙醛的組成和結(jié)構(gòu)
乙醛的分子式是C2H4O,,它的結(jié)構(gòu)式是 ,結(jié)構(gòu)簡(jiǎn)式是CH3CHO,。
講述
從結(jié)構(gòu)上看,,乙醛可以看成是甲基與醛基相連構(gòu)成的化合物。
板書
(二)乙醛的性質(zhì)
講述
乙醛是一種無色有刺激氣味的液體,,易揮發(fā),,密度比水小,,沸點(diǎn)20.8 ℃。既能溶于水,,也能溶于乙醇,、乙醚等有機(jī)溶劑。
乙醛的化學(xué)性質(zhì)表現(xiàn)在以下幾方面:
板書
1.還原反應(yīng)
講述
乙醛的分子結(jié)構(gòu)中含有醛基,。醛基中羰基的碳氧雙鍵和碳碳雙鍵一樣,,其中一個(gè)鍵不穩(wěn)定,容易發(fā)生與氫的加成反應(yīng),,生成乙醇,,反應(yīng)式如下:
Ni
△
板書
![]()
CH3CHO + H2 CH3CH2OH
 
乙醛等含有不飽和雙鍵的有機(jī)物和氫的加成反應(yīng)也叫還原反應(yīng)。
2.氧化反應(yīng)
講述
醛很容易被氧化成含相同碳原子數(shù)的有機(jī)酸,。如乙醛在加熱和催化劑作用下被氧化成乙酸,,反應(yīng)式如下:
板書
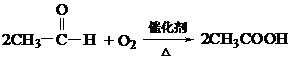
 
講述
這是工業(yè)上利用酒精制乙酸的原理。
乙醛不僅能被氧氣氧化,,還能夠被弱氧化劑氧化,。保溫瓶膽就是將銀均勻地鍍?cè)诓A闲纬傻摹?/p>
保溫瓶是重要的生活用品,保溫瓶之所以能夠保溫,,是因?yàn)槠磕懺诮Y(jié)構(gòu)上有三大特點(diǎn):一是瓶膽的瓶口做得較小,,瓶口加蓋軟木塞子,這樣可減少蒸發(fā),,防止液面上氣體的流動(dòng),,以減少熱量的散失。二是瓶膽由雙層玻璃構(gòu)成,,玻璃和軟木塞都是熱的不良導(dǎo)體,夾層里被抽成真空,,可有效地防止熱傳導(dǎo)的發(fā)生,。三是瓶膽的雙層玻璃表面上都均勻地鍍了一層銀,鍍銀的光亮表面,,能將到達(dá)表面的熱反射回去,,這樣就防止了因?yàn)闊彷椛涠鴵p失熱量。那層光亮的表面是利用銀鏡反應(yīng)制成的,,乙醛就可以發(fā)生銀鏡反應(yīng),。
板書
(1)銀鏡反應(yīng)
演示
演示教材實(shí)驗(yàn)5-8。
觀察
可以觀察到試管內(nèi)壁上附著一層光亮如鏡的金屬銀,,這個(gè)反應(yīng)叫做銀鏡反應(yīng),。
板書
![]()
AgNO3 + 3NH3·H2O Ag(NH3)2OH + NH4NO3 + 2H2O
△
![]()
CH3CHO + 2Ag(NH3)2OH CH3COONH4 + 2Ag↓+ 3NH3 + H2O
講述
銀鏡反應(yīng)可以用來檢驗(yàn)醛基的存在,工業(yè)上利用銀鏡反應(yīng)原理制造鏡子或保溫瓶膽,,生產(chǎn)上常用含有醛基的葡萄糖作為還原劑,。
板書
(2)斐林反應(yīng)
演示
演示課堂實(shí)驗(yàn)5-9,。
觀察
溶液中有磚紅色沉淀生成。
講解
實(shí)驗(yàn)中,,乙醛與斐林試劑發(fā)生了反應(yīng),,乙醛被氧化成乙酸,同時(shí)生成了磚紅色的Cu2O沉淀,,這個(gè)反應(yīng)叫做斐林反應(yīng),。
板書
![]()
CH3CHO + 2Cu(OH)2 CH3COOH + Cu2O↓ + 2H2O
講述
斐林反應(yīng)是檢驗(yàn)醛基的另一種方法。斐林試劑分A液和B液,。A液為硫酸銅溶液,,B液為氫氧化鈉的酒石酸鉀鈉溶液,使用時(shí)等體積混合,。新生成的Cu(OH)2溶解在酒石酸鉀鈉溶液中,,形成深藍(lán)色溶液。
強(qiáng)調(diào)
乙醛的化學(xué)性質(zhì)主要由醛基決定,,乙醛能夠發(fā)生加成和氧化反應(yīng),,都是發(fā)生在醛基上。
板書
(三)乙醛的用途
邊講邊板書
乙醛是重要的化工原料,,用來生產(chǎn)乙酸和三氯乙醛等,。三氯乙醛能和水加成,生成水合三氯乙醛,。水合三氯乙醛是無色晶體,,易溶于水和酒精,醫(yī)藥上用作催眠鎮(zhèn)靜劑和麻醉劑,。
投影
課堂練習(xí)
1.糖尿病患者的尿樣中含有葡萄糖,,在與新制的氫氧化銅懸濁液共熱時(shí),能產(chǎn)生磚紅色沉淀,。說明葡萄糖分子中含有( ),。
A. 羰基 B. 醛基 C. 羥基 D. 羧基
![]()
![]()
2.現(xiàn)有下列物質(zhì):
① CH3Cl , ② CCl4 ,, ③ ,, ④ ,, ⑤ CH2O
⑥C2H5OH,,⑦CH3CHO,,⑧醋酸,請(qǐng)用各物質(zhì)的序號(hào)填寫下面空白:
(1)在常溫,、常壓下為氣體的是______,。
(2)能溶于水的是______。
(3)能與鈉反應(yīng)放出H2的是______,。
(4)能與新制Cu(OH)2反應(yīng)的是______,。
(5)能發(fā)生銀鏡反應(yīng)的是______,。
過渡
前面已經(jīng)學(xué)習(xí)過醛類物質(zhì)。醛由醇氧化而得,。醛氧化后生成酸,,這三者之間存在以下相互衍生關(guān)系。
投影
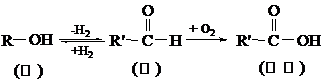
導(dǎo)入
現(xiàn)在我們學(xué)習(xí)羧酸,,它是另一類烴的衍生物,,它的代表物是乙酸。
板書
四,、乙酸
講述
乙酸是重要的有機(jī)酸,,生活中我們常接觸它。食醋是3%~5%乙酸的水溶液,,所以乙酸又叫醋酸,。下面我們先了解它的結(jié)構(gòu)。
板書
(一)乙酸的組成和結(jié)構(gòu)
展示
展示乙酸分子的模型,。
講述
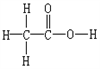
乙酸分子是由甲基和羧基組成的,。羧基是由羰基和羥基相連而成的。這兩個(gè)基團(tuán)連在一起,,相互影響,,結(jié)果不再是兩個(gè)獨(dú)立的官能團(tuán),而成為一個(gè)統(tǒng)一的整體,。所以羧基表現(xiàn)的性質(zhì)跟羥基和羰基都不同,,而是羧基特有的性質(zhì)。
板書
乙酸的分子式是C2H4O2,,結(jié)構(gòu)式是 ,,結(jié)構(gòu)簡(jiǎn)式是CH3COOH。
(二)乙酸的性質(zhì)
講述
乙酸是無色有刺激性氣味的液體,,沸點(diǎn)119.7 ℃,,熔點(diǎn)16.6 ℃,溫度低于16.6 ℃,,易凝結(jié)成冰狀固體,故稱為冰醋酸,。普通食醋中含有質(zhì)量分?jǐn)?shù)為3%~5%的乙酸,,所以乙酸又叫醋酸。乙酸與水能按任何比例混溶,,也溶于其溶劑中,。
講述
乙酸的化學(xué)性質(zhì)表現(xiàn)在以下幾方面:
板書
1.乙酸的酸性
講解
乙酸最顯著的性質(zhì)是具有酸性,能與氫氧化鈉,、碳酸氫鈉等作用生成鹽,。
板書
![]()
CH3COOH + NaHCO3 CH3COONa + CO2↑ + H2O
講解
加入無機(jī)酸又可以使鹽重新變?yōu)轸人帷?/p>
板書
![]()
CH3COONa + HCl CH3COOH + NaCl
強(qiáng)調(diào)
乙酸是一種弱酸,,但比碳酸和苯酚的酸性強(qiáng),具有酸的通性,。
板書
2.酯化反應(yīng)
講述
酸與醇作用生成酯和水的反應(yīng)叫做酯化反應(yīng),。乙酸與乙醇發(fā)生反應(yīng),生成乙酸乙酯,。
演示
演示教材實(shí)驗(yàn)5-10,,在試管里先加入3 mL乙醇,然后一邊振蕩一邊慢慢地加入2 mL濃硫酸和2 mL冰醋酸,,按教材圖5-18裝置好,。用酒精燈小心均勻地加熱試管3~5 min。
觀察
產(chǎn)生的蒸氣經(jīng)導(dǎo)管通到接受試管中的飽和碳酸鈉溶液的液面上,,并凝聚成透明的油狀液體,,可聞到水果香味。
講解
在濃H2SO4存在下,,加熱乙酸和乙醇的混合物,,會(huì)產(chǎn)生一種有香味的物質(zhì)乙酸乙酯。
板書
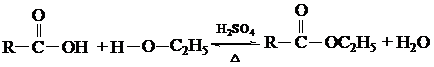
講解
乙酸乙酯是無色透明,、具有芳香氣味的液體,,可用作香料。白酒越陳越香就是因?yàn)榫浦幸掖急谎趸闪松倭恳宜?,乙醇和乙酸作用生成了具有香味的乙酸乙酯?/p>
由于乙酸乙酯在同樣的條件下,,部分水解成乙酸和乙醇,所以上述反應(yīng)是可逆的,。酯化反應(yīng)一般是酸分子中羧基上的羥基和醇羥基中的氫結(jié)合脫水生成酯的過程,。
板書
(三)乙酸的用途
講述
除食用外,乙酸是常用的有機(jī)溶劑,,也是重要的化工原料,。大量用于制造合成纖維、醫(yī)藥(如阿司匹林),、油漆和農(nóng)藥等,。
投影
課堂練習(xí)
1.下列各有機(jī)化合物都有多種官能團(tuán)
 
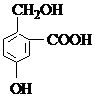
(A) 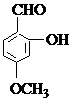
(B) (C)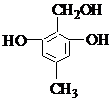
 
 
 
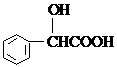
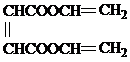
(D) (E)
 
(1)可看作醇類的是______________。
(2)可看作酚類的是_____________,。
(3)可看作羧酸類的是_____________,。
(4)可看作酯類的是______________。
分析
運(yùn)用所學(xué)的醇,、酚,、羧酸、酯的概念(普遍性結(jié)論),再基于上述有機(jī)化合物結(jié)構(gòu)中官能團(tuán)的種類和位置(個(gè)性),,略加演繹推理,,即可獲得如下結(jié)論。
小結(jié)
乙醛,、乙酸的結(jié)構(gòu)和性質(zhì),。
作業(yè)
綜合練習(xí)題一、三,、五,。
 
【板書設(shè)計(jì)】
第三節(jié) 烴的衍生物
三、乙醛
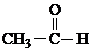
(一)乙醛的組成和結(jié)構(gòu)
分子式為C2H4O,,結(jié)構(gòu)式為 ,,結(jié)構(gòu)簡(jiǎn)式為CH3CHO。
(二)乙醛的性質(zhì)
催化劑
1.加成反應(yīng)
△
![]()
CH3CHO + H2 CH3CH2OH
乙醛等含有不飽和雙鍵的有機(jī)物和氫的加成反應(yīng)也叫還原反應(yīng),。
催化劑
2.氧化反應(yīng)
![]()
△
2CH3CHO + O2 2CH3COOH
(1)銀鏡反應(yīng)
△
![]()
AgNO3 + 3NH3·H2O Ag(NH3)2OH + NH4NO3 + 2H2O
![]()
CH3CHO + 2[Ag(NH3)2]OH H2O + 2Ag↓+ 3NH3↑+ CH3COONH4
 
△
(2)斐林反應(yīng)
![]()
CH3CHO + 2Cu(OH)2 Cu2O ↓+ 2H2O + CH3COOH
(三)乙醛的用途
四,、乙酸
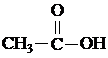
(一)乙酸的組成與結(jié)構(gòu)
分子式為C2H4O2,結(jié)構(gòu)式為 ,,結(jié)構(gòu)簡(jiǎn)式為CH3COOH,。
(二)乙酸的性質(zhì)
1. 酸性
乙酸是一種弱酸,具有酸的通性,,比碳酸和苯酚的酸性強(qiáng),。
濃硫酸
2. 酯化反應(yīng)
△
![]()
CH3COOH + CH3CH2OH CH3COOC2H5 + H2O
(三)乙酸的用途
202
 

 負(fù)責(zé)人:黃劍鵬
負(fù)責(zé)人:黃劍鵬