《化學(xué)》電子教案
 
課題 | 第三章 滴定分析法 第一節(jié) 滴定分析法概述(之二) |
教學(xué)目標(biāo) | 1. 了解定量分析誤差的表示方法 2.掌握有效數(shù)字及運(yùn)算規(guī)則 3. 了解滴定分析法的基本概念 |
教學(xué)重點(diǎn) | 有效數(shù)字及運(yùn)算規(guī)則,、滴定分析法的基本概念 |
教學(xué)難點(diǎn) | 有效數(shù)字及運(yùn)算規(guī)則 |
課時(shí)安排 | 2學(xué)時(shí) |
教學(xué)方法 | 啟發(fā)式教學(xué)與講練結(jié)合法 |
教學(xué)手段 | 多媒體輔助 |
教學(xué)用具 | 投影儀 |
 
【教學(xué)進(jìn)程】
提問
1.定量分析的一般程序包括哪幾步,?
2.系統(tǒng)誤差和偶然誤差各有什么特點(diǎn),?
引入
分析結(jié)果的準(zhǔn)確度用誤差表示,,但客觀存在的真實(shí)值不可能準(zhǔn)確知道,準(zhǔn)確表示一個(gè)實(shí)驗(yàn)結(jié)果,,實(shí)際中用的不是誤差而是偏差,。
板書
第一節(jié) 滴定分析法概述
三、誤差的表示方法
2.精密度與偏差
講解
精密度是指同一試樣的多次平行測(cè)定值之間彼此符合的程度,,常用偏差來表示,。
板書
精密度:同一試樣的多次平行測(cè)定值之間彼此符合的程度,常用偏差來表示,。
講解
我們把單次測(cè)定值與算術(shù)平均值之間的差值叫做單次測(cè)定值的絕對(duì)偏差,,簡(jiǎn)稱偏差。偏差越小,,精密度越高,;反之,,則精密度越低,。
板書
偏差:?jiǎn)未螠y(cè)定值與算術(shù)平均值之間的差值。
–
平均值 ![]()
–
―
絕對(duì)偏差 ![]()
指出
式中![]() 是單次測(cè)定值,,n是測(cè)定次數(shù),。
是單次測(cè)定值,,n是測(cè)定次數(shù),。
強(qiáng)調(diào)
為了更好地衡量一組測(cè)定值的精密度,常用相對(duì)平均偏差來表示,。
板書
–
絕對(duì)平均偏差 ![]()
–
–
相對(duì)平均偏差 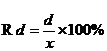
投影
例題 有位同學(xué)在實(shí)驗(yàn)之后得到了5個(gè)數(shù)據(jù):36.46,、36.48、36.43,、36.42,、36.46,計(jì)算平均值,、絕對(duì)平均偏差和相對(duì)平均偏差,。
–
解:算術(shù)平均值![]()
各次測(cè)量的絕對(duì)偏差分別為:
![]()
![]()
![]()
![]()
![]()
–
–
–
絕對(duì)平均偏差![]()
相對(duì)平均偏差![]()
 
過渡
對(duì)分析結(jié)果的評(píng)價(jià)可用準(zhǔn)確度與精密度,那么準(zhǔn)確度與精密度之間有什么關(guān)系呢,?
講解
準(zhǔn)確度表示測(cè)量的正確性,,精密度表示測(cè)量的重復(fù)性,兩者的含義不同,,不可混淆,,但相互又有制約關(guān)系。
板書
3.準(zhǔn)確度與精密度的關(guān)系
講解
精密度是保證準(zhǔn)確度的必要條件,。精密度差,,準(zhǔn)確度不可能真正好,如果精密度差而準(zhǔn)確度好,,這只是偶然巧合,,并不可靠,。
板書
(1)準(zhǔn)確度高,一定要精密度高,。
講解
精密度雖然是準(zhǔn)確度的必要條件,,但不是充分條件,因?yàn)榭赡艽嬖谙到y(tǒng)誤差,。
板書
(2)精密度高,,不一定準(zhǔn)確度高。
強(qiáng)調(diào)
對(duì)一個(gè)好的分析結(jié)果,,既要求精密度高,,又要求準(zhǔn)確度高。
思考
假如有一份藥品其有效成分的真實(shí)值是20.26%,,一位實(shí)驗(yàn)中很細(xì)心的同學(xué)甲得到的最終結(jié)果是22.68%,,另一位實(shí)驗(yàn)中有些粗心大意的同學(xué)乙得到的最終結(jié)果是20.32%,能說明同學(xué)乙的數(shù)據(jù)好嗎,?同學(xué)甲可能存在哪些問題,?
講解
有效數(shù)字是指在分析工作中實(shí)際能測(cè)量到的數(shù)字,通常包括由儀器直接讀出的全部準(zhǔn)確數(shù)字和最后一位估計(jì)的可疑數(shù)字,。記錄數(shù)據(jù)和計(jì)算結(jié)果究竟應(yīng)該保留幾位數(shù)字,,要根據(jù)測(cè)定方法和使用儀器的準(zhǔn)確程度來決定。在記錄數(shù)據(jù)和計(jì)算結(jié)果時(shí),,所保留的有效數(shù)字中,,只有最后一位是可疑數(shù)字。
板書
四,、有效數(shù)字及其運(yùn)算規(guī)則
1.有效數(shù)字
在分析工作中實(shí)際能測(cè)量到的數(shù)字,。
舉例說明
用萬分之一天平稱取試樣0.321 8 g,其最后一位“8”是可疑數(shù)字,,其真實(shí)值可能是 0.321 9 g,,也可能是0.321 7 g。再如,,常用滴定管體積的刻度(mL)可以讀到小數(shù)點(diǎn)后第二位數(shù),,所以讀常量滴定管的體積時(shí),應(yīng)讀到小數(shù)點(diǎn)后第二位,。如25.00 mL,,不能寫成25 mL或25.0 mL。
強(qiáng)調(diào)
有效數(shù)字位數(shù)的確定應(yīng)視具體情況而定,。
舉例練習(xí)
0.5 0.002% 一位有效數(shù)字
0.42 0.40% 兩位位有效數(shù)字
6.31 1.86×10-5 三位有效數(shù)字
21.05 0.500 0 四位有效數(shù)字
強(qiáng)調(diào)
“0”可以是有效數(shù)字,,也可以不是有效數(shù)字。當(dāng)“0”位于數(shù)字中間時(shí),,它是有效數(shù)字,,如21.05中的“0”是有效數(shù)字,;“0”在數(shù)字前面不是有效數(shù)字,只起定位作用,,如0.002%和0.42中的“0”都不是有效數(shù)字,;在數(shù)字后面的“0”仍屬有效數(shù)字,如0.500 0中“5”后面的三個(gè)“0”均為有效數(shù)字,。
注意
非實(shí)驗(yàn)測(cè)得數(shù)據(jù),,如自然數(shù)“10”、“1/3”,,常數(shù)“π”,、“e”等可視為無限多位的有效數(shù)字。
過渡
在處理數(shù)據(jù)時(shí),,對(duì)于一些準(zhǔn)確度不同的數(shù)據(jù),,必須按一定規(guī)則進(jìn)行計(jì)算。
板書
2.運(yùn)算規(guī)則
講解并板書
(1)記錄所測(cè)數(shù)據(jù)時(shí),,應(yīng)包括所有的準(zhǔn)確數(shù)字和最后一位可疑數(shù)字,。
(2)當(dāng)有效數(shù)字位數(shù)確定后,其余數(shù)字一律舍棄,,遵循四舍六入五成雙原則,。
講解
幾個(gè)數(shù)據(jù)相加或相減時(shí),,和或差的有效數(shù)字保留,,應(yīng)以小數(shù)點(diǎn)后位數(shù)最少的數(shù)據(jù)為準(zhǔn),如0.012 1+25.64+1.057 82=26.71,。
板書
(3)加減法則:幾個(gè)數(shù)據(jù)相加或相減時(shí),,和或差的有效數(shù)字保留,應(yīng)以小數(shù)點(diǎn)后位數(shù)最少的數(shù)據(jù)為準(zhǔn),。
講解
幾個(gè)數(shù)據(jù)相乘或相除時(shí),,積或商的有效數(shù)字的保留,應(yīng)以有效數(shù)字位數(shù)最少的數(shù)據(jù)為準(zhǔn),,如0.012 1×25.64×1.057 82=0.328,。
板書
(4)乘除法則:幾個(gè)數(shù)據(jù)相乘或相除時(shí),積或商的有效數(shù)字的保留,,應(yīng)以有效數(shù)字位數(shù)最少的數(shù)據(jù)為準(zhǔn),。
思考
假如你第一次用分析天平精確稱量了一份純度很高的藥品,得到數(shù)據(jù)為0.567 8 g,,放入一潔凈容器,;第二次又用另一臺(tái)天平稱量了一份同樣的藥品,得到數(shù)據(jù)為0.23 g,,也放入同一容器中,,這兩份藥品相加得到的數(shù)據(jù)為0.797 8 g,,你認(rèn)為這個(gè)數(shù)據(jù)準(zhǔn)確么?如果科學(xué)計(jì)量,,應(yīng)該怎樣處理,?
過渡
滴定分析法是化學(xué)分析中的一種重要的分析方法,下面我們來學(xué)習(xí)滴定分析法涉及的一些名詞,。
板書
五,、滴定分析法概述
1.有關(guān)名詞術(shù)語
講解
滴定分析法是指將一種已知準(zhǔn)確濃度的試劑溶液,通過滴定管滴加到一定量的待測(cè)組分的溶液中,,直到所加試劑與待測(cè)組分按化學(xué)計(jì)量關(guān)系反應(yīng)為止,,然后根據(jù)標(biāo)準(zhǔn)溶液的濃度和所消耗的體積,計(jì)算出待測(cè)組分的含量,。
講解并板書
(1)標(biāo)準(zhǔn)溶液:已知準(zhǔn)確濃度的試劑溶液,。
(2)試液:含待測(cè)組分的溶液。
(3)滴定:將標(biāo)準(zhǔn)溶液通過滴定管逐滴滴加到待測(cè)溶液中的操作過程,。
(4)化學(xué)計(jì)量點(diǎn):滴加的標(biāo)準(zhǔn)溶液與待測(cè)組分按化學(xué)計(jì)量關(guān)系恰好完全反應(yīng)的這一點(diǎn),。
(5)指示劑:用來確定化學(xué)計(jì)量終點(diǎn)的試劑。
(6)滴定終點(diǎn):指示劑顏色發(fā)生變化的轉(zhuǎn)變點(diǎn),。
(7)終點(diǎn)誤差:滴定終點(diǎn)與化學(xué)計(jì)量點(diǎn)兩者之間所造成的差值,。
指出
終點(diǎn)誤差的大小主要決定于指示劑的性能和用量,所以在滴定分析中,,對(duì)指示劑的選擇顯得十分重要,。
小結(jié)
1.定量分析法誤差的表示。
2.有效數(shù)字的運(yùn)算規(guī)則,。
3. 滴定分析法的基本概念,。
作業(yè)
思考與練習(xí) 2、3,、4,。
 
【板書設(shè)計(jì)】
第一節(jié) 滴定分析法概述
三、誤差的表示方法
2.精密度與偏差
精密度:同一試樣的多次平行測(cè)定值之間彼此符合的程度,,常用偏差來表示,。
偏差:?jiǎn)未螠y(cè)定值與算術(shù)平均值之間的差值。
–
平均值 ![]()
–
–
絕對(duì)偏差 ![]()
–
絕對(duì)平均偏差 ![]()
–
–
–
相對(duì)平均偏差 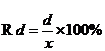
3.準(zhǔn)確度與精密度的關(guān)系,。
(1)準(zhǔn)確度高,,一定要精密度高。
(2)精密度高,,不一定準(zhǔn)確度高,。
四、有效數(shù)字及其運(yùn)算規(guī)則
1.有效數(shù)字
在分析工作中實(shí)際能測(cè)量到的數(shù)字。
2.運(yùn)算規(guī)則,。
(1)記錄所測(cè)數(shù)據(jù)時(shí),,應(yīng)包括所有的準(zhǔn)確數(shù)字和最后一位可疑數(shù)字。
(2)當(dāng)有效數(shù)字位數(shù)確定后,,其余數(shù)字一律舍棄,,遵循四舍六入五成雙原則。
(3)加減法則:幾個(gè)數(shù)據(jù)相加或相減時(shí),,和或差的有效數(shù)字保留,,應(yīng)以小數(shù)點(diǎn)后位數(shù)最少的數(shù)據(jù)為準(zhǔn)。
(4)乘除法則:幾個(gè)數(shù)據(jù)相乘或相除時(shí),,積或商的有效數(shù)字的保留,,應(yīng)以有效數(shù)字位數(shù)最少的數(shù)據(jù)為準(zhǔn)。
五,、滴定分析法概述
1.有關(guān)名詞術(shù)語
(1)標(biāo)準(zhǔn)溶液:已知準(zhǔn)確濃度的試劑溶液,。
(2)試液:含待測(cè)組分的溶液。
(3)滴定:將標(biāo)準(zhǔn)溶液通過滴定管逐滴滴加到待測(cè)溶液中的操作過程,。
(4)化學(xué)計(jì)量點(diǎn):滴加的標(biāo)準(zhǔn)溶液與待測(cè)組分按化學(xué)計(jì)量關(guān)系恰好完全反應(yīng)的這一點(diǎn),。
(5)指示劑:用來確定化學(xué)計(jì)量終點(diǎn)的試劑。
(6)滴定終點(diǎn):指示劑顏色發(fā)生變化的轉(zhuǎn)變點(diǎn),。
(7)終點(diǎn)誤差:滴定終點(diǎn)與化學(xué)計(jì)量點(diǎn)兩者之間所造成的差值,。
89
 

 負(fù)責(zé)人:黃劍鵬
負(fù)責(zé)人:黃劍鵬